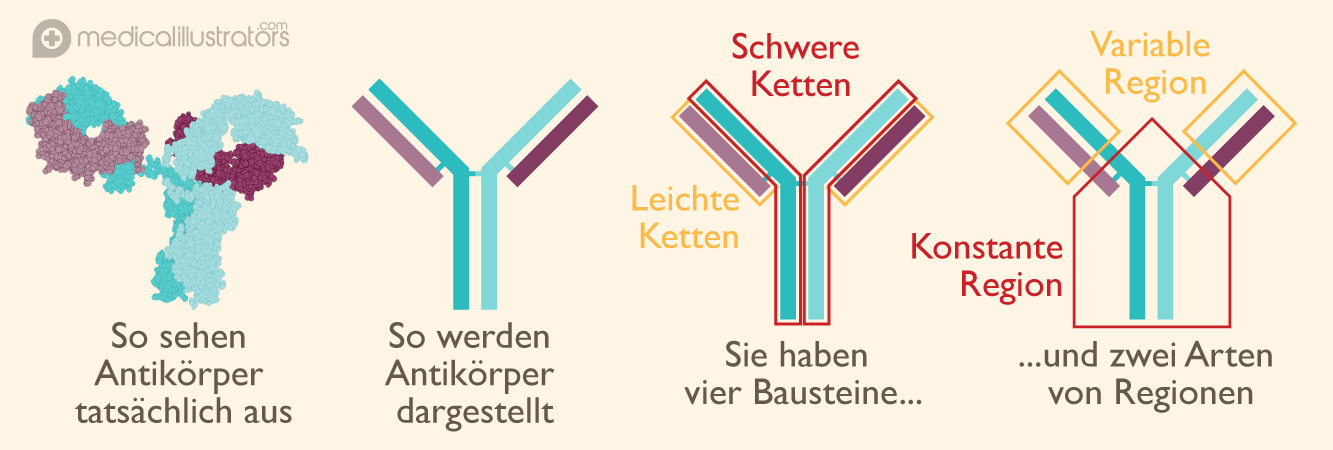
Antikörper sind Moleküle, die aus vier Bausteinen bestehen: zwei grossen, den sogenannten schweren Ketten, und zwei kleinen, den sogenannten leichten Ketten. Neben dieser Struktur aus leichten und schweren Ketten verfügen alle Antikörper über zwei Regionen. Eine davon ist bei allen Antikörpern ganz ähnlich aufgebaut: die konstante Region – der Teil, der zur Aktivierung des Immunsystems verwendet wird – und eine, die das Immunsystem aktiviert. Die andere, die variable Region, kann unzählige verschiedene Formen annehmen und so zahlreiche unterschiedliche Erreger erkennen.
Neue Behandlungsmöglichkeiten – Monoklonale Antikörper
Fachartikel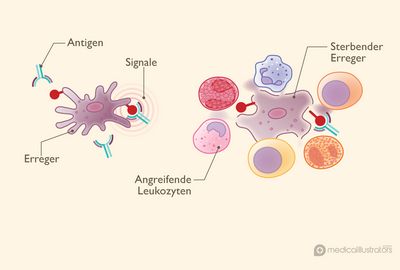
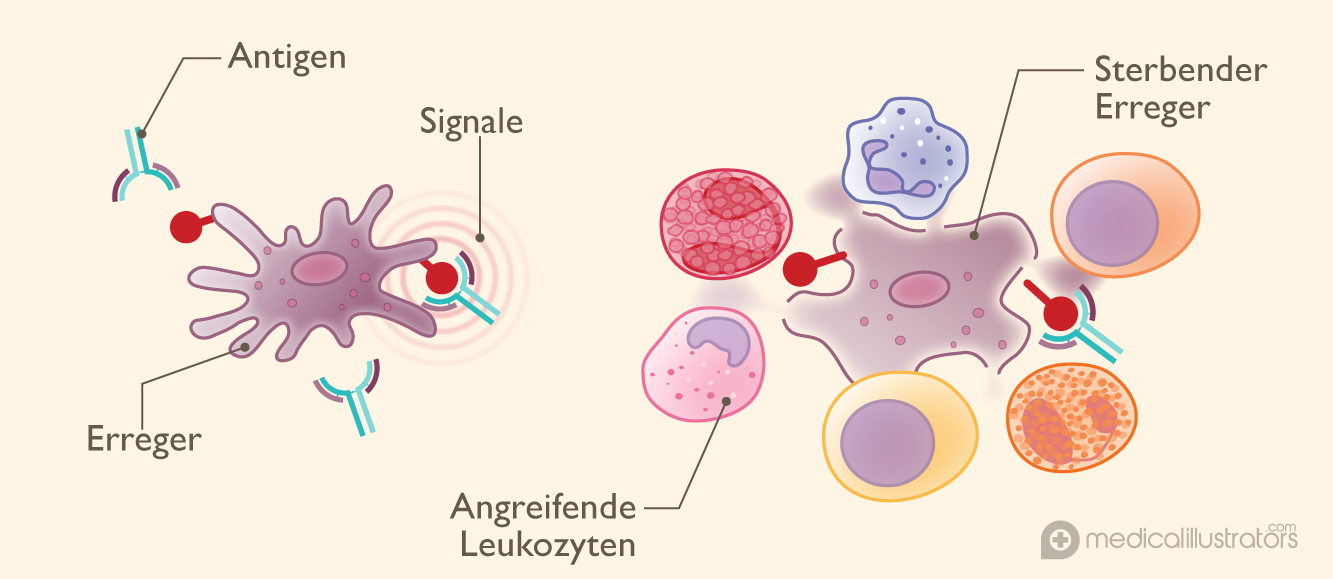
Dank der Fähigkeit der Antikörper, verschiedene Formen anzunehmen, können sie viele verschiedene Arten von Gefahrensignalen –Die vielen verschiedenen variablen Regionen sind jeweils für die Erkennung eines bestimmten Gefahrensignals zuständig, eines sogenannte Antigens, unten im Bild rot dargestellt. So erkennt das Immunsystem verschiedenste Erreger und entartete Zellen und hält sie davon ab, Schaden anzurichten.
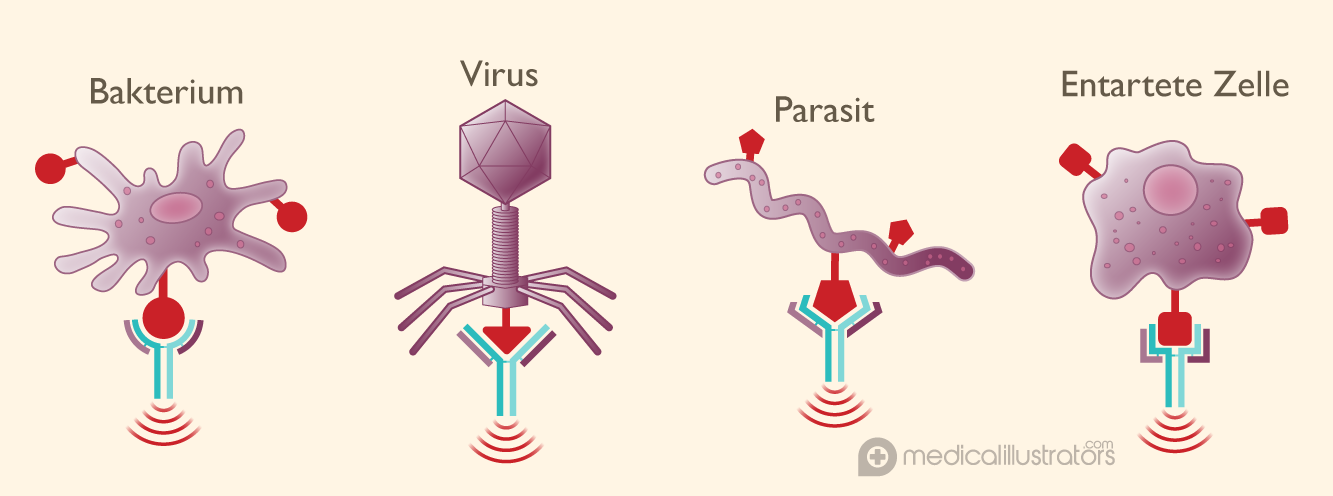
Angeregt von dieser erfolgreichen Angriffsabwehr haben Wissenschaftler nach Strategien dafür gesucht, Antikörper auch gegen Krankheiten wie beispielsweise Multiple Sklerose (MS) einzusetzen.
Was sind therapeutische monoklonale Antikörper?
Monoklonale Antikörper sind im Labor hergestellte, künstliche Antikörper, die so gestaltet sind, dass sie auch solche Gefahrensignale erkennen, die den natürlichen Antikörpern entgehen. Therapeutische monoklonale Antikörper sind darauf ausgerichtet, jeweils ein spezifisches Antigen zu erkennen, das typisch für eine bestimmte Erkrankung ist.
Wenn sie in den Blutkreislauf eines Patienten injiziert werden, verhalten sich die monoklonalen Antikörper genau wie die natürlichen Antikörper: Sie patrouillieren im Körper und suchen nach bestimmten Gefahrensignalen. Sobald sie diese gefunden haben, aktivieren sie die körpereigenen Abwehrmechanismen zur Bekämpfung der Krankheit.
Diese Technologie ist sehr vielversprechend, da sie neue Möglichkeiten zur Bekämpfung von Krankheiten bietet, die immer noch schwer behandelbar sind wie Krebs, rheumatoide Arthritis, Psoriasis, Morbus Crohn, MS usw.
Gegenwärtig sind zwei monoklonale Antikörper zur Behandlung von MS zugelassen: Natalizumab (Tysabri®) und Alemtuzumab (Lemtrada®). Weitere monoklonale Antikörper werden in klinischen Studien geprüft (Ocrelizumab, Daclizumab).
Wie wirken monoklonale Antikörper gegen MS?
Weisse Blutkörperchen, die auch Leukozyten genannt werden, sind Immunzellen, die für die Bekämpfung der inneren und äusseren Angreifer zuständig sind. Sie sind in 6 Klassen unterteilt, die sich in ihrer Grösse, in ihrer Form und in den an ihrer Oberfläche präsentierten Molekülen unterscheiden und jeweils eigene Namen haben, wie in der folgenden Abbildung dargestellt.
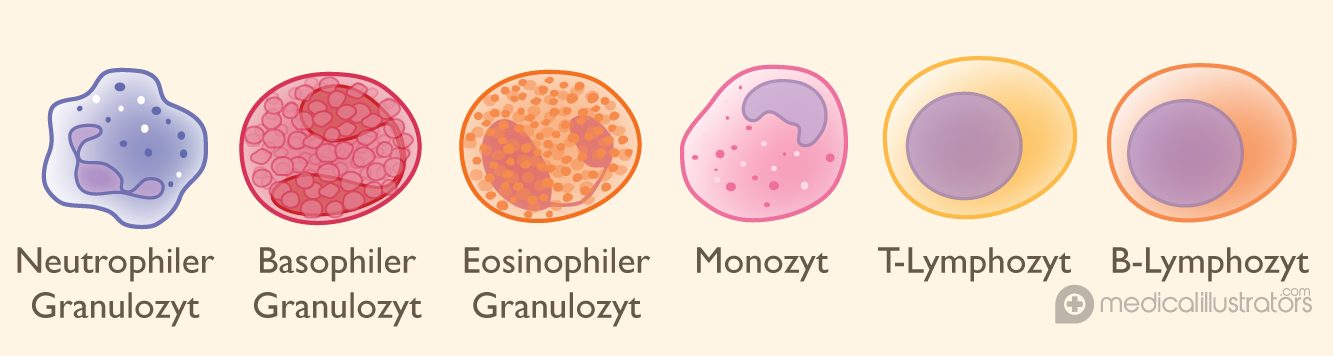
Unter normalen Umständen bemerken die im Blutstrom zirkulierenden Leukozyten, wenn ein Gewebe angegriffen wird. Sie durchdringen die Barriere, die sie von dem angegriffenen Gewebe trennt, und setzen eine Reihe entzündlicher Reaktionen in Gang, die die Bedrohung, tote und beschädigte Zellen entfernen und die Heilung des Gewebes ermöglichen.
Bei Menschen mit MS dringen anomale Leukozyten ohne einen solchen Anlass aus dem Blutkreislauf in Gehirn und Rückenmark ein und lösen dort unnötige Entzündungsreaktionen aus. Diese Entzündung zerstört die wichtige Myelinschicht der Nervenzellen, aus denen Gehirn und Rückenmark aufgebaut sind, und beeinträchtigt so deren Funktion.
Die Symptome von Menschen mit MS sind die Folge dieser anomalen Immunreaktion. Monoklonale Antikörper gegen MS sind darauf ausgerichtet, die Entzündungsreaktionen im Gehirn und Rückenmark, dem sogenannten zentralen Nervensystem, einzudämmen. Dazu werden verschiedene Ansätze genutzt:
Natalizumab
Um die Schranke zwischen Blutkreislauf und zentralem Nervensystem überwinden zu können, verfügen Leukozyten über bestimmte Marker an ihrer Oberfläche, die sogenannten Adhäsionsmoleküle. Natalizumab wurde so gestaltet, dass der Antikörper sich fest an diese Moleküle bindet und es den Leukozyten so unmöglich macht, eine Entzündungsreaktion im zentralen Nervensystem auszulösen, die zur MS führt.
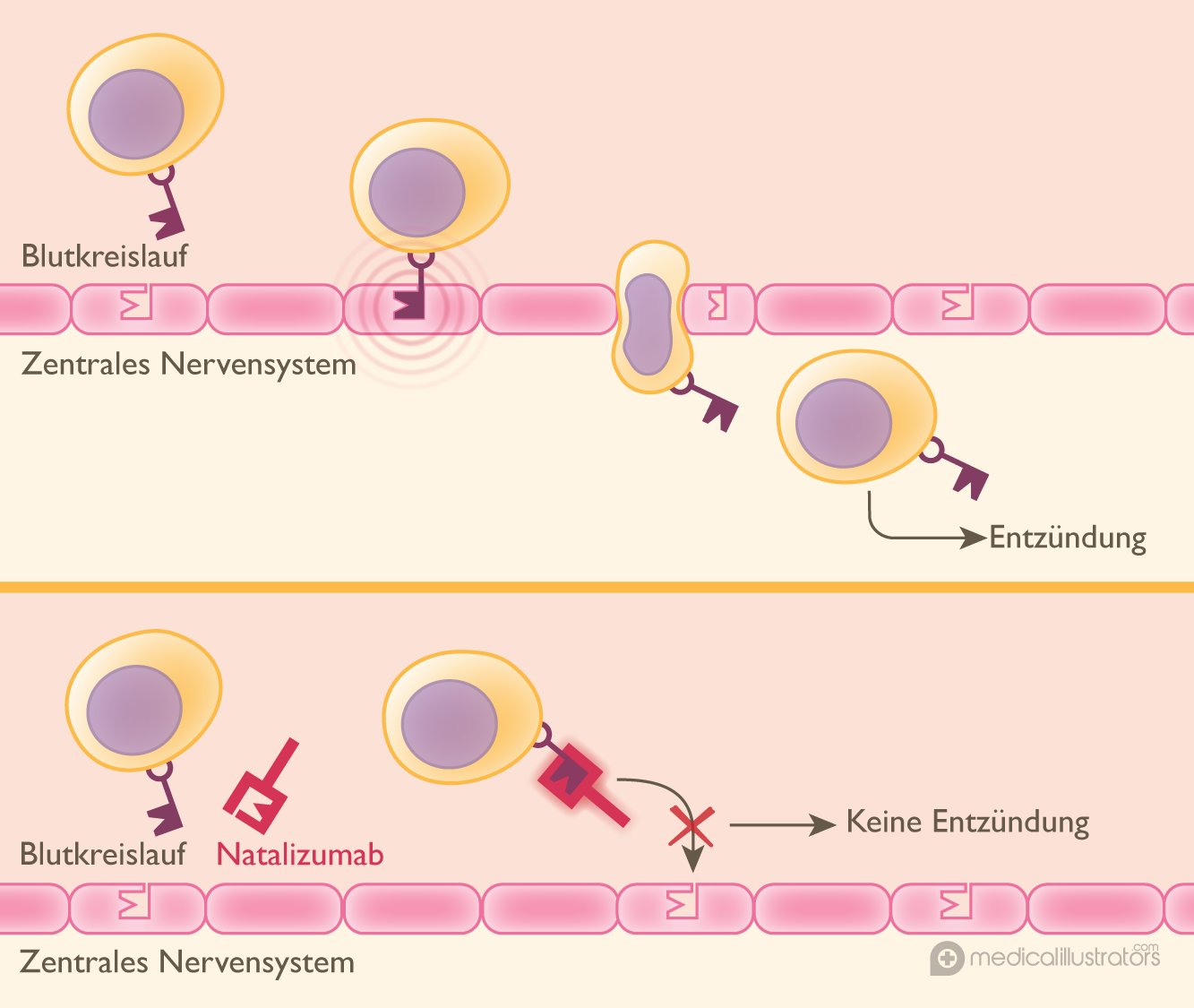
Natalizumab ist in der Schweiz zur Behandlung schubförmig remittierender, sekundär progredienter und progredient schubförmiger MS zugelassen. Die Verordnung muss von einer engmaschigen Überwachung begleitet werden, da seltene, aber schwerwiegende Nebenwirkungen beobachtet wurden.
Alemtuzumab
Lymphozyten sind diejenigen Leukozyten, die die ersten Signale zur Auslösung der Entzündungsreaktionen im zentralen Nervensystem senden. Alemtuzumab wurde so gestaltet, dass es speziell an einen Marker auf der Oberfläche von Lymphozyten bindet. Durch diesen an die Lymphozyten gebunden Antikörper werden diese Zellen für die Vernichtung durch das körpereigene Immunsystem gekennzeichnet.
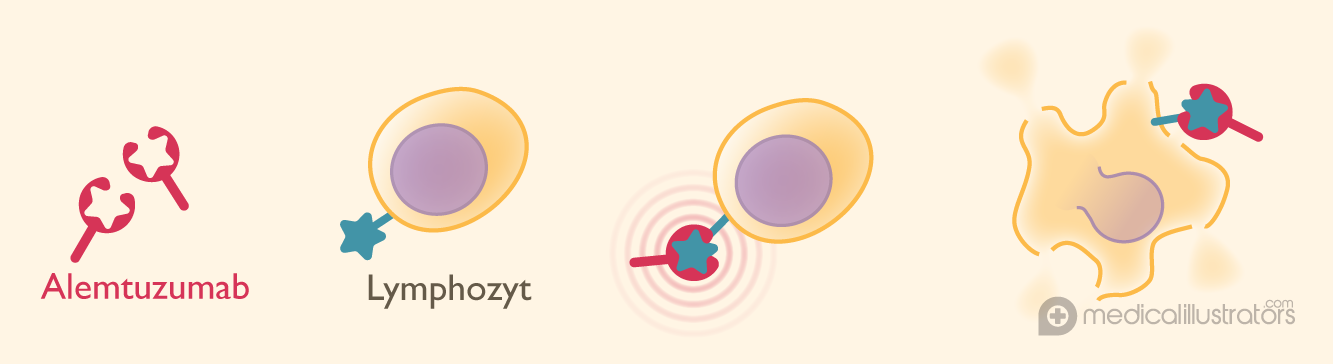
Alemtuzumab ist in der Schweiz zur Behandlung erwachsener Patienten mit aktiver schubförmig remittierender MS oder nach Therapieversagen zugelassen. Da noch keine Langzeitsicherheitsdaten vorliegen, sind regelmässige Besuche beim verordnenden Arzt unverzichtbar.
Ocrelizumab und Daclizumab
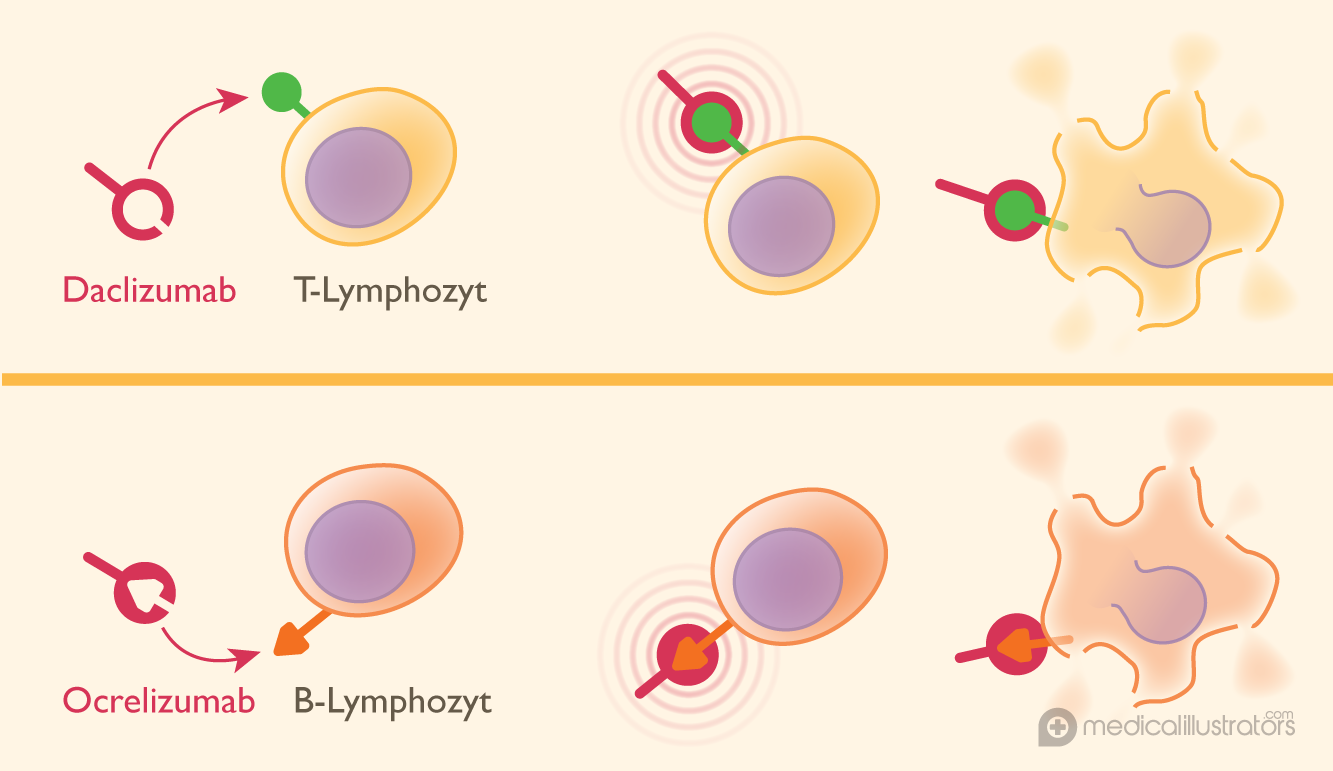
Es gibt zwei Arten von Lymphozyten: B-Lymphozyten und T-Lymphozyten. Beide tragen zu der Entzündung bei, die die Symptome von MS-Patienten auslöst.
Ocrelizumab erkennt einen Marker, der charakteristisch für B-Lymphozyten ist, während Daclizumab darauf ausgerichtet ist, einen Marker auf der Oberfläche von T-Lymphozyten zu erkennen. Ähnlich wie bei Alemtuzumab werden mit Ocrelizumab markierte B-Lymphozyten und mit Daclizumab markierte T-Lymphozyten vom Immunsystem zerstört und können keinen Entzündungsprozess im zentralen Nervensystem mehr auslösen.
Ocrelizumab wird gegenwärtig in klinischen Studien (Phase III) im Vergleich zu Rebif (Interferon β) bei Patienten mit schubförmiger MS geprüft. Ergebnisse sind im Jahr 2019 zu erwarten.
Daclizumab hat im Vergleich zu Rebif positive Ergebnisse bei Patienten mit schubförmig remittierender MS (Phase-III-Studie) gezeigt. Die Sicherheit dieses monoklonalen Antikörpers wird gegenwärtig noch genauer untersucht. Die Endergebnisse werden im Jahr 2017 erwartet.
Dr. Lutz Achtnichts